Запис рівняння через масу і щільність газу
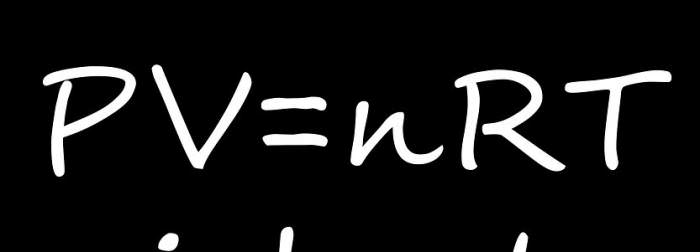
Вище на малюнку записано рівняння ідеального газу. У ньому фігурує кількість речовини n. Однак на практиці часто відома змінна або постійна маса ідеального газу m. В цьому випадку рівняння запишеться у такій формі:
P * V = m / M * R * T.
M – молярна маса для даного газу. Наприклад, для кисню O2 вона дорівнює 32 г/моль.
Нарешті, перетворюючи останній вираз можна переписати так:
P = ρ / M * R * T
Де ρ – щільність субстанції.
Суміш газів
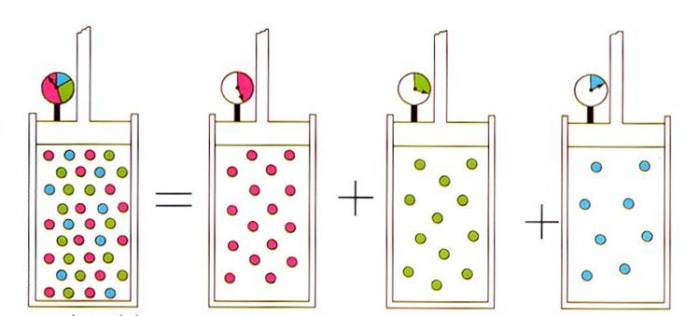
Суміш ідеальних газів описується так званим законом Дальтона. Цей закон випливає з рівняння ідеального газу, яке застосовне для кожного компоненту суміші. Дійсно, кожний компонент займає весь об’єм і має однакову з іншими компонентами суміші температуру, що дозволяє записати:
P = ∑iPi = R * T / V * ∑ini.
Тобто повне тиск в суміші P дорівнює сумі парціальних тисків Pi всіх компонент.