Закони Шарля і Гей-Люссака
Ці закони математично описують ізобарний і ізохорний процеси, тобто такі переходи між станами газової системи, при яких зберігаються тиск і об’єм, відповідно. Закон Шарля математично можна записати наступним чином:
V/T = const при n, P = const.
Закон Гей-Люссака записується так:
P/T = const при n, V = const.
Якщо обидва рівності представити у вигляді графіка, то ми отримаємо прямі лінії, які під деяким кутом нахилені до осі абсцис. Такий вид графіків говорить про прямий пропорційності між об’ємом і температурою при постійному тиску і між тиском і температурою при постійному обсязі.
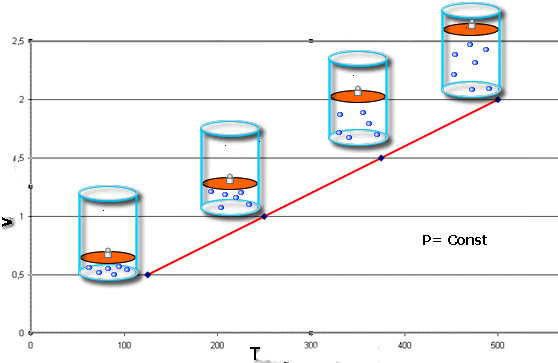
Відзначимо, що всі три розглянутих газових закону не беруть до уваги хімічний склад газу, а також зміна його кількості речовини.
Абсолютна температура
У побуті ми звикли користуватися температурною шкалою Цельсія, оскільки вона є зручною для опису оточуючих нас процесів. Так, вода кипить при температурі 100 oC, а замерзає при 0 oC. У фізиці ця шкала виявляється незручною, тому застосовують так звану абсолютну шкалу температур, яка була введена лордом Кельвіном в середині XIX століття. Відповідно до цієї шкали температура вимірюється в Кельвінах (К).
Вважається, що при температурі -273,15 oC не існує ніяких теплових коливань атомів і молекул, припиняється повністю їх поступальний рух. Цієї температури в градусах Цельсія відповідає абсолютний нуль в Кельвінах (0 До). З цього визначення випливає фізичний сенс абсолютної температури: вона є мірою кінетичної енергії складають матерію частинок, наприклад, атомів або молекул.
Крім наведеного вище фізичного сенсу абсолютної температури, існують інші підходи до розуміння цієї величини. Одним з них є згаданий газовий закон Шарля. Запишемо його в наступній формі:
V1/T1 = V2/T2 =>
V1/V2 = T1/T2.
Останнє рівність говорить про те, що при певній кількості речовини в системі (наприклад, 1 моль) і певному тиску (наприклад, 1 Па) обсяг газу однозначно визначає абсолютну температуру. Іншими словами, зростання обсягу газу при зазначених умовах можливо тільки за рахунок збільшення температури, а зменшення обсягу свідчить про зменшення величини T.
Нагадаємо, що на відміну від температури за шкалою Цельсія, абсолютна температура не може приймати від’ємні значення.