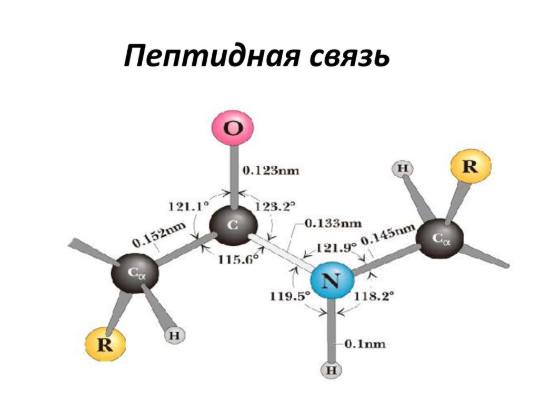
Що це внутрішня енергія газу?
Перш ніж записати формулу внутрішньої енергії ідеального газу, необхідно познайомитися з цією характеристикою ближче.
В термодинаміці внутрішню енергію, як правило, позначають латинською буквою U. Визначається в загальному випадку вона за наступною формулою:
U = H – P*V
Де H – ентальпія системи, P і V – тиск і об’єм.
За своїм фізичним змістом внутрішня енергія складається з двох складових: кінетичної і потенційної. Перша пов’язана з різного роду рухом частинок системи, а друга – з силовим взаємодією між ними. Якщо застосувати це визначення до концепції ідеального газу, у якого відсутня потенційна енергія, то величина U при будь-якому стані системи буде точно дорівнює його кінетичній енергії, тобто:
U = Ek.
Висновок формули внутрішньої енергії
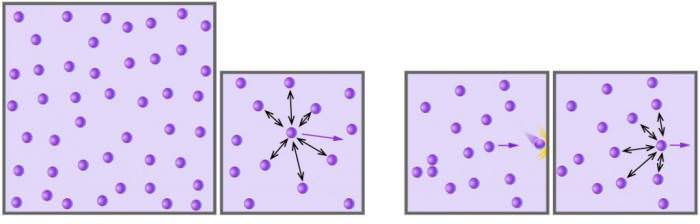
Вище ми встановили, що для її визначення у системи з ідеальним газом необхідно розрахувати його кінетичну енергію. З курсу загальної фізики відомо, що енергія частинки масою m, яка поступально рухається в певному напрямку зі швидкістю v, визначається за формулою:
Ek1 = m*v2/2.
Її також можна застосувати для газових частинок (атомів і молекул), однак, необхідно зробити деякі зауваження.
По-перше, під швидкістю v слід розуміти деяку середню величину. Справа в тому, що газові частинки рухаються з різними швидкостями відповідно до розподілу Максвелла-Больцмана. Останнє дозволяє визначити середню швидкість, яка з плином часу не змінюється, якщо відсутні зовнішні впливи на систему.
По-друге, формула для Ek1 передбачає енергію на одну ступінь свободи. Газові частинки можуть рухатися у всіх трьох напрямках, а також обертатися в залежності від їх будови. Щоб врахувати величину ступеня свободи z, її слід помножити на Ek1, тобто:
Ek1z = z/2*m*v2.
Кінетична енергія всієї системи Ek в N разів більше, ніж Ek1z, де N – загальна кількість газових частинок. Тоді для U отримуємо:
U = z/2*N*m*v2.
Згідно цій формулі, зміна внутрішньої енергії газу можливо тільки в тому випадку, якщо поміняти число частинок N в системі, або їх середню швидкість v.