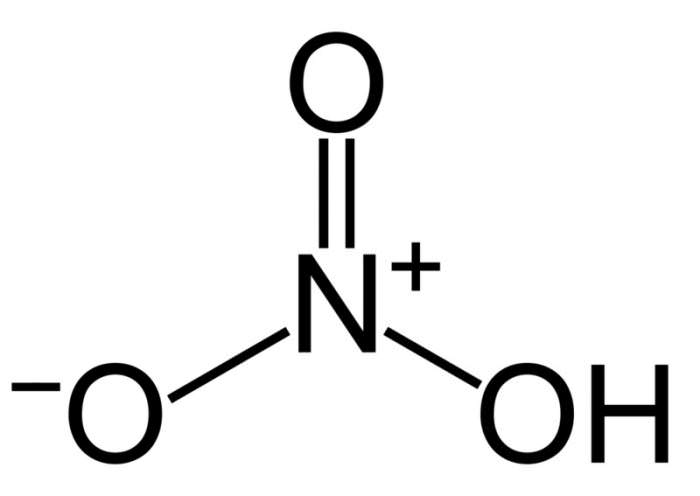
Азотна кислота (HNO3)
Азотна кислота поставляється у вигляді концентрованого розчину (68-70 %, 16 М) і в безводній формі (100 %). Це сильний окислювач. Властивості зберігаються, навіть якщо він достатньо розведений і знаходиться при кімнатній температурі. Це речовина окисляє більшість органічних сполук, перетворюючись у закис азоту. Вона може утворювати вибухонебезпечні суміші практично з будь-яким органічним з’єднанням.
Концентрована азотна кислота бурхливо реагує з органічним матеріалом, що призводить до виділення газу і потенційного підвищення тиску, після чого відбувається розрив посудини, якщо ємність не вентилюється належним чином. Реакції окислення з деякими органічними розчинниками можуть утворювати вибухонебезпечні нітрати.
Азотна кислота вступає у взаємодію з більшістю металів, виділяючи або газоподібний водень, або оксиди азоту залежно від концентрації і виду реагенту. Вона не розчиняє золото і платину.
Змішування азотної і соляної кислоти призведе до утворення коричневих пари, що складаються з токсичних оксидів азоту.
Речовина викликає виникнення жовтих плям на шкірі.