При вирішенні термодинамічних задач з фізики, в яких виникають переходи між різними станами ідеального газу, рівняння Менделєєва-Клапейрона є важливою опорною точкою. У цій статті розглянемо, що це за рівняння і як їм можна користуватися при вирішенні практичних завдань.
Реальні та ідеальні гази

Газове стан матерії являє собою одне з існуючих чотирьох агрегатних станів речовини. Прикладами чистих газів є водень і кисень. Гази можуть змішуватися один з одним в довільних пропорціях. Всім відомий приклад суміші – повітря. Названі гази є реальними, однак за певних умов вони можуть вважатися ідеальними. Ідеальним вважається газ, який відповідає наступним характеристикам:
- Частинки, що утворюють його, не взаємодіють один з одним.
- Зіткнення між окремими частинками і між частинками і стінками судин носять абсолютно пружний характер, тобто кількість руху і кінетична енергія до і після зіткнення зберігається.
- Частинки не володіють об’ємом, але мають деяку масу.
Всі реальні гази при температурах порядку та вище кімнатної (більше 300 К) і при тисках порядку і нижче однієї атмосфери (105 Па) можна вважати ідеальними.
Описують стан газу термодинамічні величини
Під термодинамічними величинами розуміють макроскопічні фізичні характеристики, які однозначно визначають стан системи. Існує три базові величини:
- температура T;
- обсяг V;
- тиск P.
Температура відображає інтенсивність руху атомів і молекул в газі, тобто вона визначає кінетичну енергію частинок. Вимірюється ця величина в Кельвінах. Для перекладу з градусів Цельсія Кельвины слід використовувати рівність:
T(K) = 273,15 + T(oC).
Обсяг – здатність кожного реального тіла або системи займати частину простору. Виражається в СІ в метрах кубічних (м3).
Тиск – макроскопічна характеристика, яка в середньому описує інтенсивність зіткнень частинок газу зі стінками посудини. Чим більше температура і вище концентрація частинок, тим більше буде тиск. Виражається воно в паскалях (Па).
Далі буде показано, що рівняння Менделєєва-Клапейрона у фізиці містить ще один макроскопічний параметр – кількість речовини n. Під ним вважають число елементарних одиниць (молекул, атомів), яке дорівнює числу Авогадро (NA = 6,02 * 1023). Виражається кількість речовини в молях.
Рівняння стану Менделєєва-Клапейрона
Запишемо відразу це рівняння, а потім пояснимо його значення. Це рівняння має наступний загальний вигляд:
P * V = n * R * T.
Добуток тиску на об’єм ідеального газу є пропорційною добутку кількості речовини в системі на абсолютну температуру. Коефіцієнт пропорційності R називається універсальною газовою сталою. Її значення дорівнює 8,314 Дж/(моль*К). Фізичний зміст величини R полягає в тому, що вона дорівнює роботі, яку здійснює при розширенні 1 моль газу в разі його нагрівання на 1 К.
Записане вираз також називається рівнянням стану ідеального газу. Його важливість полягає в тому, що воно не залежить від хімічного типу частинок газу. Так, це можуть бути молекули кисню, атоми гелію або взагалі газова повітряна суміш, для всіх цих речовин буде справедливо розглянуте рівняння.
Воно може бути записано в інших формах. Наведемо їх:
P * V = m / M * R * T;
P = ρ / M * R * T;
P * V = N * kB * T.
Тут m – маса газу, ρ – щільність, M – молярна маса, N – число частинок в системі, kB – стала Больцмана. В залежності від умови задачі можна використовувати будь-яку форму запису рівняння.
Коротка історія отримання рівняння

Рівняння Клапейрона-Менделєєва вперше було отримано в 1834 році Емілем Клапейроном в результаті узагальнення законів Бойля-Маріотта і Шарля-Гей-Люссака. При цьому закон Бойля-Маріотта був відомий вже в другій половині XVII століття, а закон Шарля-Гей-Люссака вперше був опублікований на початку XIX століття. Обидва закони описують поведінку закритої системи при фіксованому одному термодинамічний параметр (температури або тиску).
Заслуга Д. Менделєєва при запису сучасної форми рівняння ідеального газу полягає в тому, що він вперше замінив ряд констант однією єдиною величиною R.

Відзначимо, що в даний час рівняння Клапейрона-Менделєєва може бути отримано теоретично, якщо розглянути систему з точки зору статистичної механіки та застосувати положення молекулярно-кінетичної теорії.
Окремі випадки рівняння стану
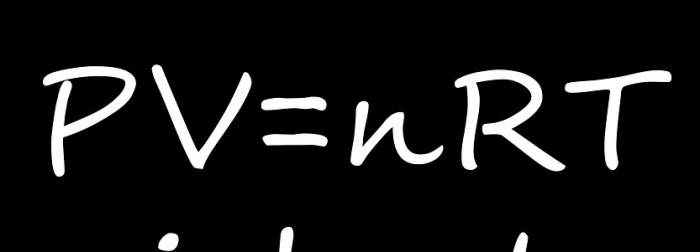
Існує 4 приватних закону, які випливають з рівняння стану ідеального газу. Зупинимося коротко на кожному з них.
Якщо в закритій системі з газом підтримувати постійну температуру, то будь-яке збільшення в ній тиску викличе пропорційне зменшення обсягу. Цей факт може бути записаний математично в такому вигляді:
P * V = const при T, n = const.
Цей закон носить прізвища вчених Роберта Бойля і Эдма Маріотта. Графіком функції P(V) є гіпербола.
Якщо в закритій системі зафіксувати тиск, то будь-яке збільшення температури в ній призведе до пропорційного зростання обсягу, тобто:
V / T = const при P, n = const.
Описаний цим рівнянням процес називається изобарным. Він носить прізвища французьких вчених Шарля і Гей-Люссака.
Якщо в закритій системі об’єм не змінюється, то процес переходу між станами системи називається изохорным. Під час нього будь-яке підвищення тиску призводить до аналогічного підвищення температури:
P / T = const при V, n = const.
Це рівняння отримало назву закону Гей-Люссака.
Графіками изобарного і ізохорний процесів є прямі лінії.
Нарешті, якщо зафіксувати макроскопічні параметри (температуру і тиск), тоді всяке збільшення кількості речовини в системі призведе до пропорційного зростання його обсягу:
n / V = const при P, T = const.
Ця рівність називається принципом Авогадро. Воно лежить в основі закону Дальтона для ідеальних газових сумішей.
Рішення завдання
Рівняння Менделєєва-Клапейрона зручно використовувати для вирішення різних практичних завдань. Наведемо приклад однієї з них.
Кисень масою 0,3 кг знаходиться в балоні об’ємом 0,5 м3 при температурі 300 К. Як зміниться тиск газу, якщо збільшити температуру До 400 к?
Вважаючи кисень в балоні ідеальним газом, скористаємося рівнянням стану для обчислення початкового тиску, маємо:
P1 * V = m / M * R * T1;
P1 = m * R * T1 / (M * V) = 0,3 * 8,314 * 300 / (32 * 10-3 * 0,5) = 46766,25 Па.
Тепер обчислимо тиск, при якому газ буде перебувати в балоні, якщо підняти температуру До 400 к, отримуємо:
P2 = m * R * T2 / (M * V) = 0,3 * 8,314 * 400 / (32 * 10-3 * 0,5) = 62355 Па.
Зміна тиску при нагріванні складе:
ΔP = P2 – P1 = 62355 – 46766,25 = 15588,75 Па.
Отримане значення ΔP відповідає 0,15 атмосфери.