Термодинаміка – це самостійний розділ фізики, який вивчає процеси переходу між станами системи, оперуючи при цьому макроскопічними характеристиками. Одним з важливих об’єктів вивчення термодинаміки є ідеальний газ. Дана стаття присвячена розгляду концепції ідеального газу і одиниць вимірювання універсальної газової сталої.
Ідеальний газ
Газове агрегатний стан матерії характеризується хаотичним розташуванням частинок, відстань між якими значно більше їх розмірів. Ці частинки знаходяться в постійному русі, тому газ не зберігає свою форму і свій обсяг.
Ідеальним газом називається будь-яка речовина, розмірами частинок якого і взаємодіями між якими можна знехтувати. В рамках концепції ідеального газу вважають, що будь-які зіткнення частинок зі стінками посудини носять абсолютно пружний характер. Середня кінетична енергія часток однозначно визначає температуру ідеального газу.
Більшість реальних газів, які знаходяться при не дуже високих тисках і не дуже низьких температурах, можна вважати з високою точністю ідеальними.
Універсальне рівняння стану
Так називають рівняння, яке об’єднує в рамках одного виразу всі важливі термодинамічні параметри ідеальної газової системи. Запишемо його:
P*V = n*R*T.
Тут P і V – тиск у паскалях і об’єм в кубічних метрах, n і T – кількість речовини в молях і температура системи в Кельвінах. Це рівняння називається рівнянням або законом Клапейрона-Менделєєва в честь французького фізика і інженера і російського хіміка XIX століття, які вивели це рівняння з накопиченого попередніми поколіннями вчених експериментального досвіду.

Універсальне рівняння стану системи дозволяє отримати будь-газовий закон. Наприклад, закон Гей-Люссака випливає з нього безпосередньо, якщо покласти постійним обсяг під час термодинамічного процесу.
Вище ми розшифрували 4 з 5 позначень, присутніх у формулі. П’ятим є коефіцієнт R. Він називається універсальною газовою сталою. Одиницею вимірювання в СІ для нього є джоуль на моль-кельвін (Дж/(моль*К)). Що це за величина, розглянемо докладніше далі в статті.
Постійна R у фізиці
Вище ми побачили, що це деякий коефіцієнт пропорційності між тиском, об’ємом, температурою і кількістю речовини. Одиницею виміру універсальної газової сталої в системі СІ є Дж/(моль*К). Її значення з точністю до трьох знаків після коми одно 8,314. Це число означає, що один моль ідеального газу, будучи нагрітим на 1 кельвін, в процесі свого розширення зробить роботу 8,314 джоуля.
Постійну R можна також інтерпретувати дещо інакше: якщо витратити на нагрів одного моль газу енергію в 8,314 джоуля, то його температура зросте на 1 кельвін. Іншими словами, R характеризує зв’язок між енергією і температурою для фіксованої кількості речовини.
Зауважимо, що величина R у фізиці не є базовою (фундаментальної) константою такий, як швидкість світла або постійна Планка. Тому з допомогою вибору відповідної температурної шкали і кількості частинок в системі можна домогтися того, що R буде дорівнює 1.
Вперше постійну R ввів у фізику Д. І. Менделєєв, замінивши нею в універсальному рівнянні стану Клапейрона ряд інших констант. Зазначимо, що хоча величина R введена для газів, у сучасній фізиці вона використовується також в рівняннях Дюлонга і Пті, Клаузиуса-Mossotti, Нернста та в деяких інших.

Постійні kB R
Люди, які знайомі з фізикою, могли помітити, що існує ще одна постійна величина, яка у всіх фізичних рівняннях виступає в якості переказного коефіцієнта між енергією і температурою. Ця величина називається постійної Больцмана (kB). Вона дорівнює 1,38*10-23 Дж/К. Очевидно, що повинна існувати математичний зв’язок між kB R. Такий зв’язок дійсно існує, вона має наступний вигляд:
R = kB*NA.
Тут NA – це величезне число, яке називається числом Авогадро. Одно воно 6,02*1023. Якщо кількість частинок системи дорівнює NA, то говорять, що система містить 1 моль речовини.
Таким чином, постійна Больцмана і універсальна газова стала, по суті, це один і той же перевідний коефіцієнт між температурою і енергією з тією лише різницею, що kB використовується для мікроскопічних процесів, а R – для макроскопічних.
Рішення завдання
Після знайомства з одиницями вимірювання універсальної газової сталої пропонується отримати їх з універсального рівняння для ідеального газу, яке було наведено у статті. Нижче на малюнку зображено це рівняння.
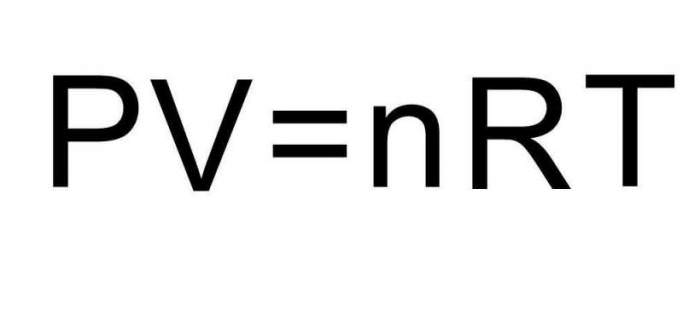
Виразимо з нього величину R, отримуємо:
R = P*V/(n*T).
Тепер підставимо для кожної фізичної величини відповідну одиницю виміру та спростимо отриманий вираз:
[R] = [Па*м3/(моль*К)] = [Н/м2*м3/(моль*К)] = [Н*м/(моль*К)] = [Дж/(моль*К)].
Як видно, при отриманні одиниць вимірювання для R ми спрощували тільки одиниці вимірювання чисельника. Спочатку була використана формула для тиску, а потім твір одиниць сили на одиниці відстані були перетворені в одиниці роботи.