Ізобарний процеси і ізохорний
Обидва процеси були спеціально винесені в один пункт статті, оскільки вони описуються математичними виразами однієї форми.
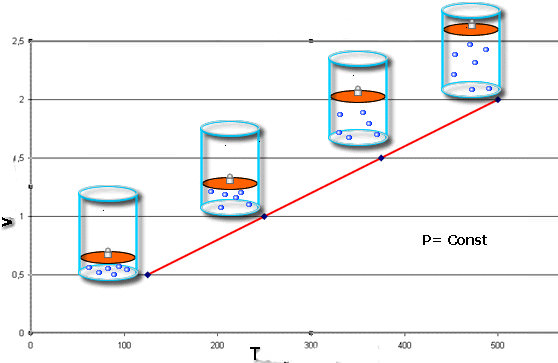
Якщо газова система розширюється або стискається, зберігаючи постійний тиск, то говорять про изобарном процесі. В такому випадку користуються наступною формулою:
V/T = const при P = const.
Цей вираз може бути отримано з рівняння стану. Воно називається законом Шарля (прізвище француза, який відкрив закон в кінці XVIII століття).
Тепер припустимо, що ми почали нагрівати газ у твердому закритій посудині. Обсяг при цьому буде залишатися постійним. Що буде відбуватися з температурою і тиском в системі? Експерименти і рівняння стану кажуть, що ці величини будуть рости пропорційно один одному, тобто:
P/T = const при V = const.
Описаний процес називається изохорным, а закон, що відображає його, названий на честь француза Гей-Люссака, який першим вивчив експериментально і опублікував на початку XIX століття.
З наведених формул випливає, що їх графічне зображення в осях V-T (изобар) і P-T (изохора) являє собою прямолінійну залежність. Приклад ізобари показаний нижче.