Формула тиску з рівняння стану

У середині 30-х років XIX століття французький інженер Еміль Клапейрон, узагальнюючи накопичений до нього експериментальний досвід з вивчення поведінки газів під час різних изопроцессов, одержав рівняння, яке в даний час називається універсальним рівнянням стану ідеального газу. Відповідна формула має вигляд:
P*V = n*R*T
Тут n – кількість речовини в молях, T – температура по абсолютній шкалі (в кельвінах). Величина R називається універсальною газовою сталою, яка була введена в це рівняння російським хіміком Д. І. Менделєєвим, тому записане вираз також називають законом Клапейрона-Менделєєва.
З рівняння вище легко отримати формулу тиску газу:
P = n*R*T/V
Рівність говорить про те, що тиск лінійно зростає з температурою при постійному об’ємі і збільшується по гіперболі з зменшенням обсягу при постійній температурі. Ці залежності відображені в законах Гей-Люссака і Бойля-Маріотта.
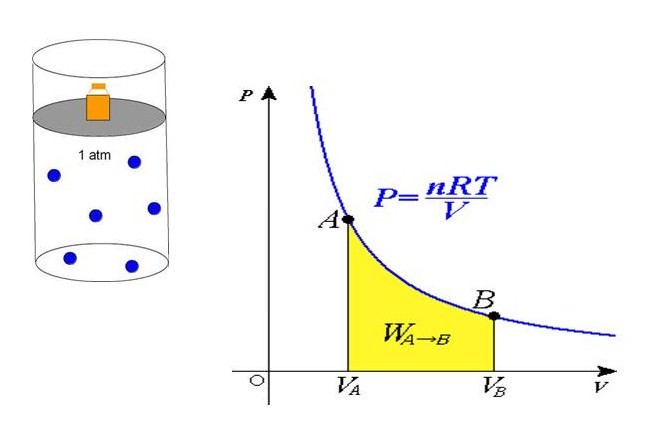
Якщо порівняти цей вираз з записаної вище формулою, яка випливає з положень МКТ, то можна встановити зв’язок між кінетичною енергією однієї частки або всієї системи і абсолютною температурою.