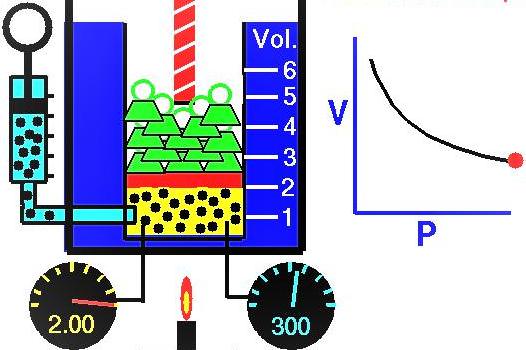
Закон Клапейрона-Менделєєва
Під час аналізу, з погляду МКТ, поведінки газу в рівновазі можна отримати наступне рівняння, яке пов’язує основні термодинамічні параметри системи:
P * V = n * R * T.
Тут тиск, об’єм і температура позначені латинськими літерами P, V і T відповідно. Величина n – це кількість речовини, яка дозволяє визначити число частинок в системі, R – газова постійна, що не залежить від хімічної природи газу. Вона дорівнює 8,314 Дж/(К*моль), тобто ідеальний газ в кількості 1 моль при його нагріванні на 1 К, розширюючись, здійснює роботу 8,314 Дж.
Записане рівність називається універсальним рівнянням стану Клапейрона-Менделєєва. Чому? Назване воно на честь французького фізика Еміля Клапейрона, який в 30-е роки XIX століття, вивчаючи встановлені до цього експериментальні газові закони, записав його у загальному вигляді. Згодом Дмитро Менделєєв привів його до сучасної формі, ввівши константу R.