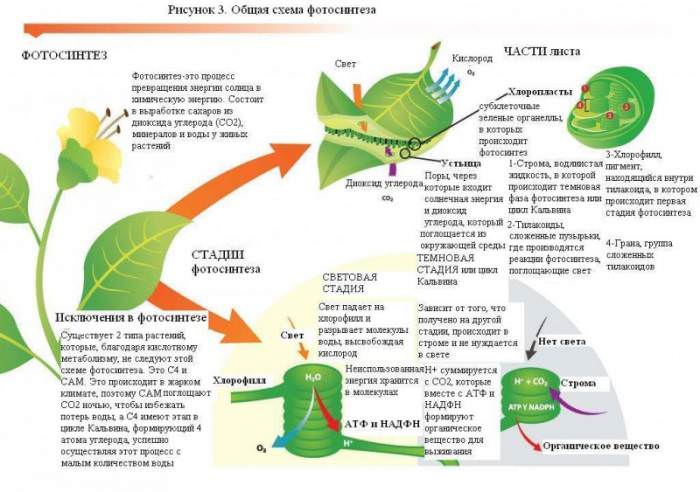
Борогидрид натрію – це речовина, що володіє високою реакційною здатністю. Дослідження його властивостей дозволило значно збагатити органічну і неорганічну хімію інформацією, а також вирішити ряд важливих аналітичних завдань. Ця сполука є одним з найбільш промислово освоєних серед усіх борогидридов металів лужно-земельної групи.
Загальний опис
Борогидрид натрію являє собою безбарвна кристалічна речовина без запаху. На відміну від інших борогидридов лужних металів, воно володіє відносною стійкістю на повітрі і у воді. Цим зумовлено його широке застосування в хімічній промисловості.
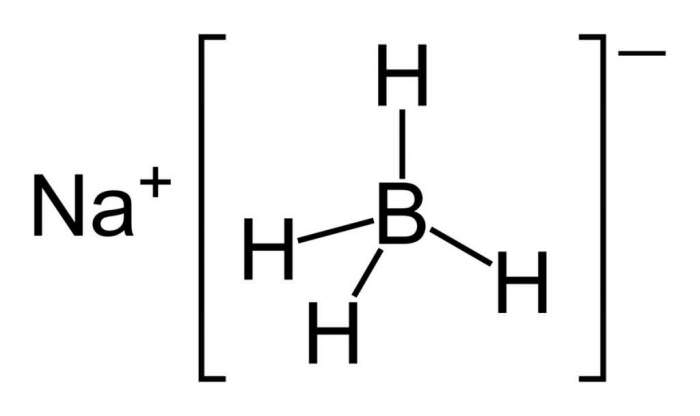
Емпірична формула борогидрида натрію має вигляд: Nabh 4.
Фізичні властивості
Для даного з’єднання характерні такі фізичні властивості:
- температура плавлення – 500 °С;
- вид кристалічної решітки – кубічна сингония;
- молекулярна маса – 37,843 а. е. м.;
- щільність – 1,08 кг/м3;
- гігроскопічність – висока;
- висока електрична провідність в розчині з аміаком і диглимом.

Хімічні властивості
Основними хімічними властивостями борогидрида натрію є наступні:
- хороша розчинність в воді, спиртах, рідкому аміаку, похідних аміаку і оксокислот; погана – в діетиловому ефірі, вуглеводневих з’єднаннях;
- у неводних розчинах спостерігається обмінна реакція з галогенідами літію, магнію, барію, алюмінію;
- з води речовина кристалізується у формі дигідрату Nabh 4-2H2O;
- при реагуванні з азотом відбувається відновлення аміаку;
- висушування дигідрату можна зробити лише в умовах вакууму;
- в реакції з диметилформамидом, ацетамидом відбувається утворення сольватов.
Ця речовина володіє високою реакційною і відновною здатністю. Другий тип процесу йде при різних параметрах:
- відсутність розчинника;
- у водних розчинах;
- в органічних середовищах;
- в розчинах з широким діапазоном кислотно-лужного показника.
Отримання

Синтез цього з’єднання проводиться декількома способами. Основні типи реакцій описані нижче:
- диборан з гідридом або метилатом натрію:
2NaH + B2H6 → 2NaBH4 ,
3CH3ONa + 2B2H6 → 3NaBH4 + B(OCH3)3;
- диметоксиборан з триметоксиборогидридом натрію:
2NaBH(OCH3)3 + 3(CH3O)2BH3= Nabh 4 + 3B(OCH3)3;
- гідриду натрію з борноэтиловым ефіром:
4NaH + B(OCH2CH3)3 → Nabh 4 + 3NaOCH2CH3;
- гідрид натрію з трихлоридом бору або борним ангідридом:
BX3 + 4NaH → Nabh 4 + 3NaX ,
X = Cl, 1/2 * O.
Отримане технічне речовину піддають очищенню за допомогою екстракції або перекристалізації з різних розчинників.
Застосування
Борогидрид натрію використовують у наступних цілях:
- тонкий неорганічний та органічний синтез;
- одержання золів металів;
- дослідження будови речовин;
- визначення кінетики хімічних реакцій;
- отримання борогидридов інших металів та їх похідних;
- регенерація благородних металів (платини, паладію, срібла, золота) з відпрацьованих водних розчинів, які є продуктами лабораторного аналізу або промислового виробництва;
- отримання чистого газоподібного водню;
- спінювання синтетичних матеріалів на основі поліестерів, полівінілового спирту та пінопласту;
- синтез сполук бору (диборану, трийодида бору, гидразинмоноборана, этиламинборана, боросульфида натрію та інших);
- отримання пористих теплоізолюючих покриттів.
В якості каталізаторів для виділення водню з борогидрида у воді застосовують таблетки з щавлевої, лимонної, бурштинової кислоти, гидросульфатов, гидрофосфатов, вугілля з покриттям з солей кобальту, платини або паладію.
Металеві покриття
Борогидрид натрію використовується також для отримання покриттів типу «метал-бор», що відрізняються хорошими експлуатаційними характеристиками:
- висока твердість;
- зносостійкість;
- корозійна стійкість;
- висока температура плавлення.
Борогидридный метод дозволяє виготовити покриття при невисокій температурі (близько 40 °С) на основі міді, срібла, золота, заліза, нікелю, кобальту, паладію, платини та інших металів. В якості добавок можна використовувати різні компоненти (сульфіти, сульфіти, тіосульфати), що дає можливість отримати дво – і трикомпонентні сплави з новими властивостями.