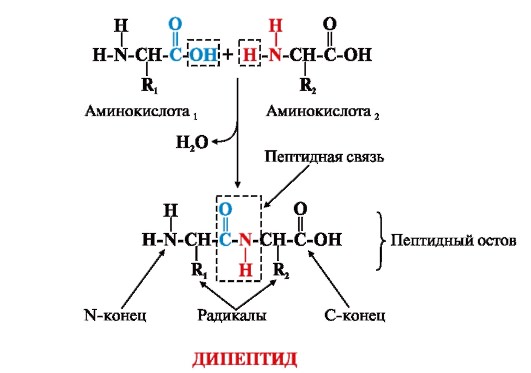
Тип амідній зв’язку, яка виникає в процесі утворення білків пептидів після взаємодій двох амінокислот, це і є відповіддю на питання, що таке пептидний зв’язок.
З пари амінокислот з’являється дипептид, тобто ланцюг з цих амінокислот, плюс молекула води. За такою ж системою відбувається генерація ланцюжків достовірніше з амінокислот у рибосом, тобто поліпептидів і білків.
Властивості ланцюжка
Різні амінокислоти, що є свого роду “будівельним матеріалом” для білка, мають радикал R.
Як і з будь-якими амідами, пептидний зв’язок ланцюга білка C-N з допомогою взаємодії канонічних структур між карбонільним вуглецем і азотним атомом, як правило, має властивість подвійний. Зазвичай це знаходить вияв у зниженні її довжини до 1,33 ангстрема.
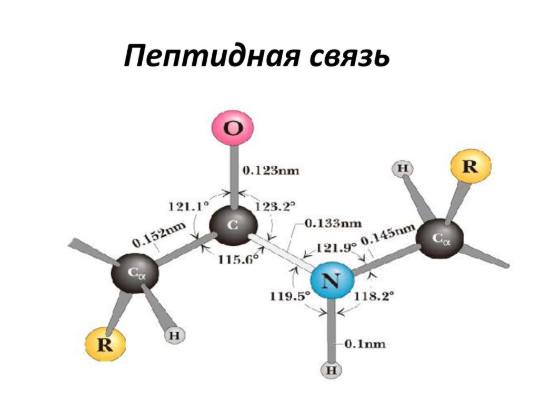
Все це веде до наступним висновків:
- C, H, O, N – 4 зв’язкових атома, плюс 2 a-вуглецю розташовуються на одній площині. Групи R амінокислот і a-вуглецеві водні розташовуються вже за межами цієї зони.
- Н О в пептидного зв’язку амінокислот і a-вуглеці пари амінокислот є транс-орієнтованими, хоча транс-ізомер більш стабільний. У L-амінокислот R-групи теж є транс-орієнтованими, що присутня у всіх пептидах і білках в природі.
- Обертання навколо ланцюжка C-N складно, більш імовірно обертання у зв’язку C-C.
Для того щоб зрозуміти, що таке пептидний зв’язок, а також для виявлення самих пептидів з білками і визначення їх кількості в певному розчині, користуються биуретовой реакцією.